Обращение медицинских изделий в Эквадоре регулируется специальным государственным агентством, а также рядом нормативно-правовых актов. Все медицинские изделия, выводимые на рынок Эквадора, должны быть зарегистрированы в соответствии с требованиями законодательства этого государства.
За регулирование обращения медицинских изделий в Эквадоре отвечает Национальное Агентство по Регулированию, Контролю и Надзору в Сфере Здравоохранения (Agencia Nacional de Regulación, Control y Vigilancia Sanitaria - ARCSA). Регистрация медицинских изделий в Эквадоре осуществляется в соответствии с требованиями Агентства.
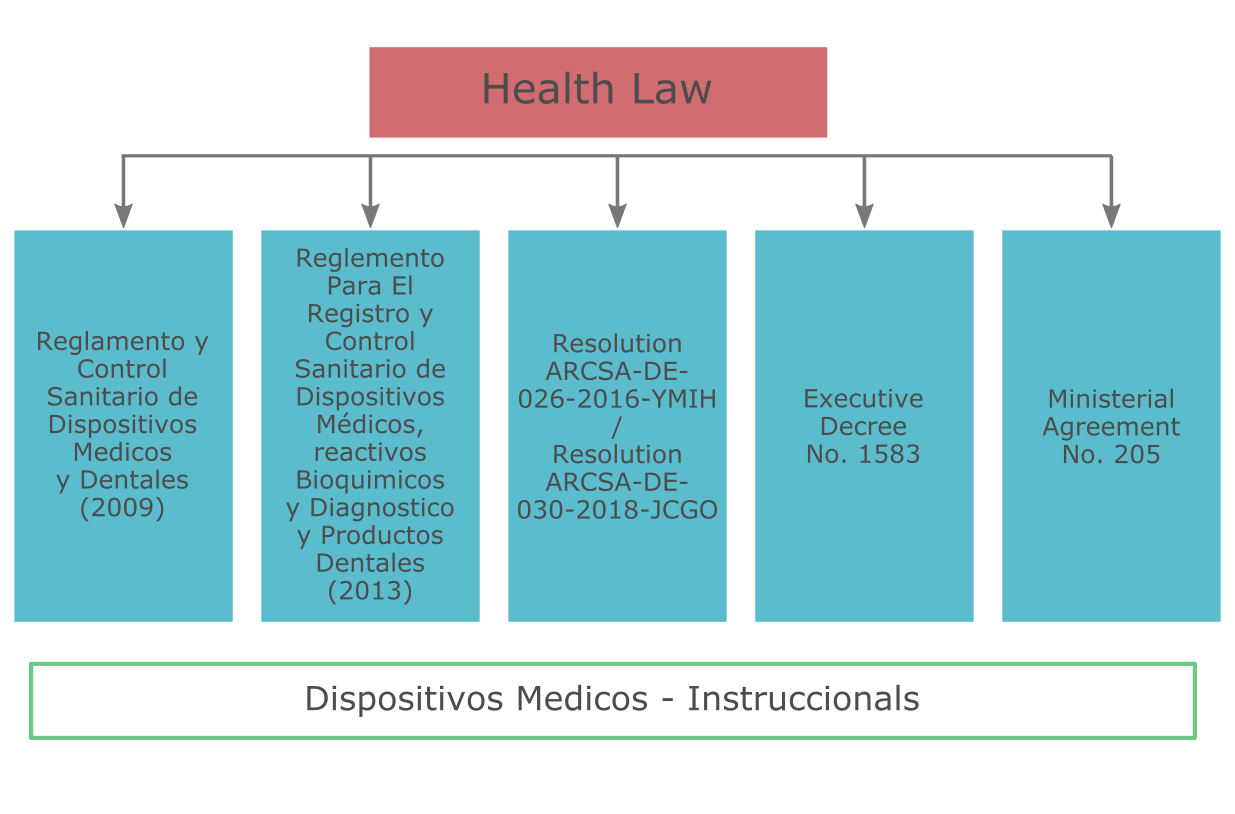
Регистрация и обращение медицинских изделий в Эквадоре регулируется Законом о Здравоохранении и целым рядом нормативно-правовых актов:
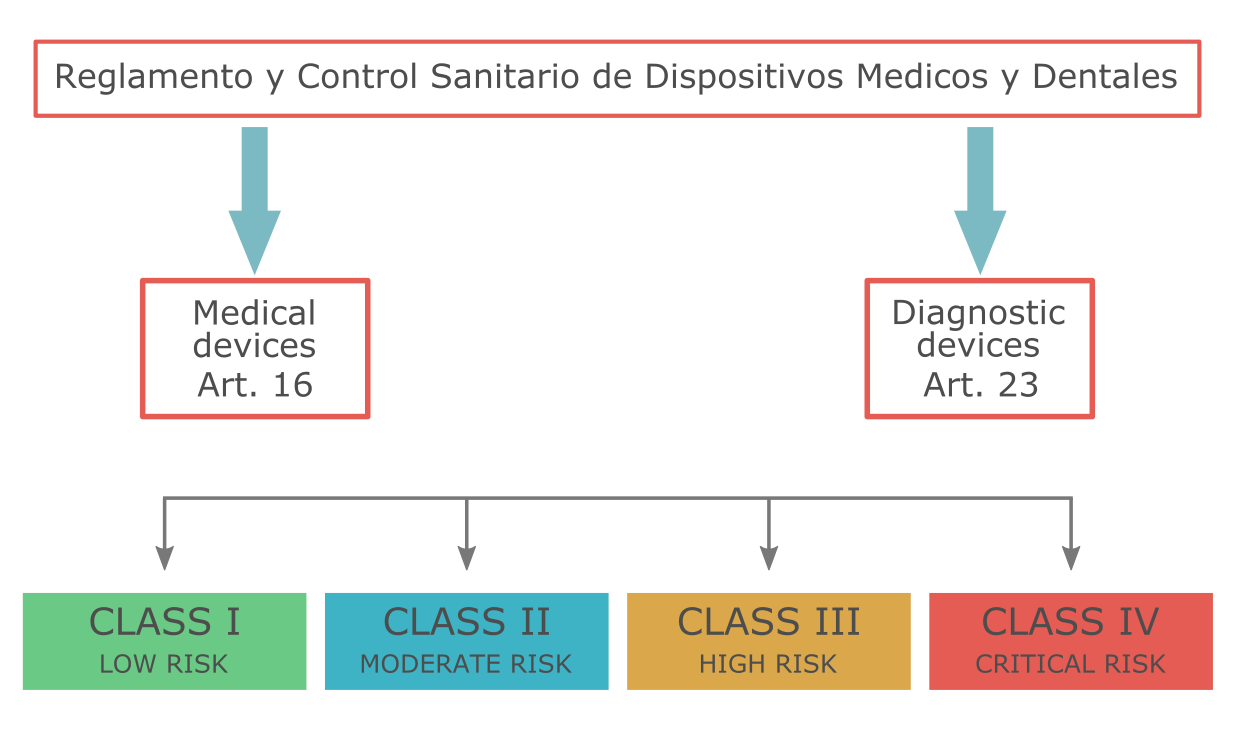
Классификация медицинских изделий в Эквадоре основана на рисках, связанных с применением медицинского изделия и опирается на правила, изложенные в статье 16 Reglamento y Control Sanitario de Dispositivos Medicos y Dentales (2009). Согласно этому документу в Эквадоре выделяют четыре класса изделий: I, II, III, IV.
Продукты для диагностики подразделяют на те же четыре класса. Но правила определения классов для них отличаются. Эти правила изложены в статье 23 указанного Регламента.
Для регистрации медицинского изделия в Эквадоре, необходимо подать в ARCSA следующую информацию.
За регистрацию медицинского изделия ARCSA взимает пошлину в размере 904.34 долларов США.
Мы здесь, чтобы помочь вам вывести вашу продукцию медицинского назначения на внешние рынки.
+357 22253765
info@mdrc-consulting.com
Обращение медицинских изделий в Эквадоре регулируется специальным государственным агентством, а также рядом нормативно-правовых актов. Все медицинские изделия, выводимые на рынок Эквадора, должны быть зарегистрированы в соответствии с требованиями законодательства этого государства.
За регулирование обращения медицинских изделий в Эквадоре отвечает Национальное Агентство по Регулированию, Контролю и Надзору в Сфере Здравоохранения (Agencia Nacional de Regulación, Control y Vigilancia Sanitaria - ARCSA). Регистрация медицинских изделий в Эквадоре осуществляется в соответствии с требованиями Агентства.
Регистрация и обращение медицинских изделий в Эквадоре регулируется Законом о Здравоохранении и целым рядом нормативно-правовых актов:

Классификация медицинских изделий в Эквадоре основана на рисках, связанных с применением медицинского изделия и опирается на правила, изложенные в статье 16 Reglamento y Control Sanitario de Dispositivos Medicos y Dentales (2009). Согласно этому документу в Эквадоре выделяют четыре класса изделий: I, II, III, IV.
Продукты для диагностики подразделяют на те же четыре класса. Но правила определения классов для них отличаются. Эти правила изложены в статье 23 указанного Регламента.

Для регистрации медицинского изделия в Эквадоре, необходимо подать в ARCSA следующую информацию.
За регистрацию медицинского изделия ARCSA взимает пошлину в размере 904.34 долларов США.
Мы здесь, чтобы помочь вам вывести вашу продукцию медицинского назначения на внешние рынки.
+357 22253765
info@mdrc-consulting.com
Мы будем рады обсудить ваш новый проект!